化石能源的大量使用带来的如温室效应等全球性环境问题,近年来越来越受到政府和科学家的关注。利用CO2作为可再生的丰富的C1源合成甲酸(HCOOH)、甲醇(MeOH)或其他碳氢化合物是发展可持续能源化学技术的关键战略。过渡金属配合物催化CO2加氢是CO2转化的一条绿色、经济的有效途径,同时也面临着巨大的挑战。北京化工大学计算化学研究所雷鸣课题组研究了Leitner等报道的[Mn(Ph2PCH2SiMe2)2N(CO)2]催化剂用来催化CO2加氢反应,发现此类催化剂具有催化CO2加氢的巨大潜力(Dalton Trans., 2021, 50: 7348-7355; Inorg. Chem., 2022, 61(14): 5616-5625; Phys. Chem. Chem. Phys., 2022, 24(21): 13365-13375)。近期,雷鸣和杨作银课题组通过密度泛函理论(DFT)方法计算在Leitner报道的Mn催化剂的基础上构建了含Si的Pincer配体的Ru-PNP(PNP=(Me2PCH2SiMe2)2N)催化剂,提出该钌配合物具有潜在的高催化加氢活性,并讨论了溶剂和不同配体的影响,相关成果已全文发表在Dalton Trans.上(https://doi.org/10.1039/D2DT01352E)。
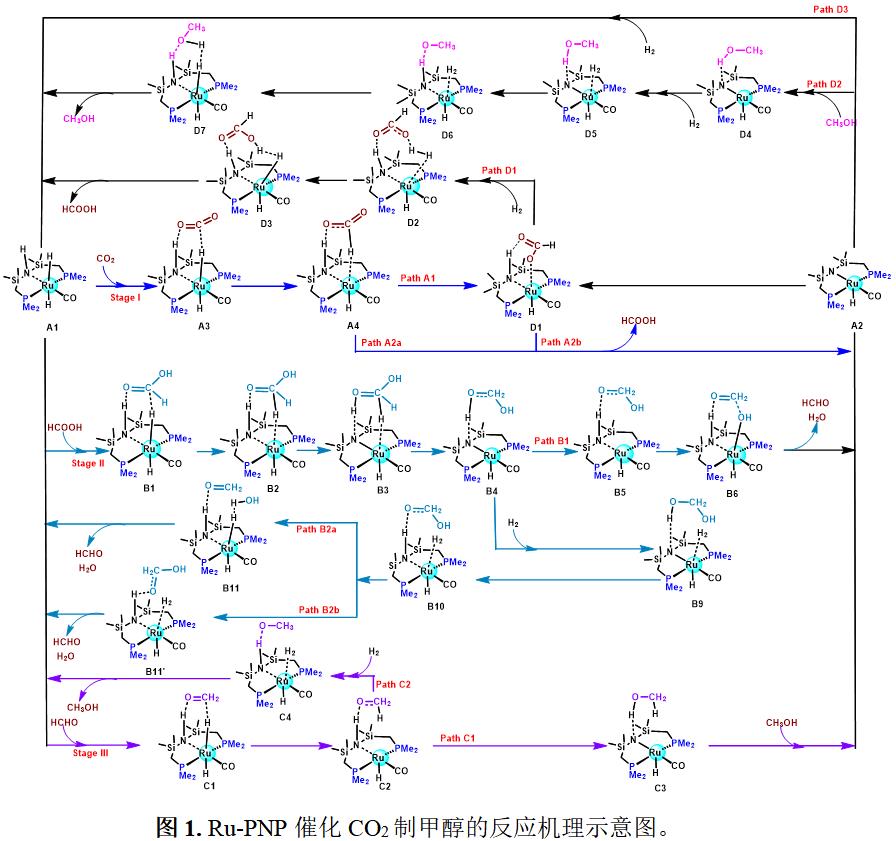
如图1所示,本文采用DFT方法探究了探讨了Ru-PNP配合物A1催化CO2加氢反应机理,整个催化级联反应由三个催化循环组成:CO2加氢为甲酸,甲酸加氢为甲醛,甲醛加氢为甲醇。每个催化循环均包括两个步骤:通过氢转移步骤完成CO2/HCOOH/HCHO的加氢,以及催化活性物质A1的再生。
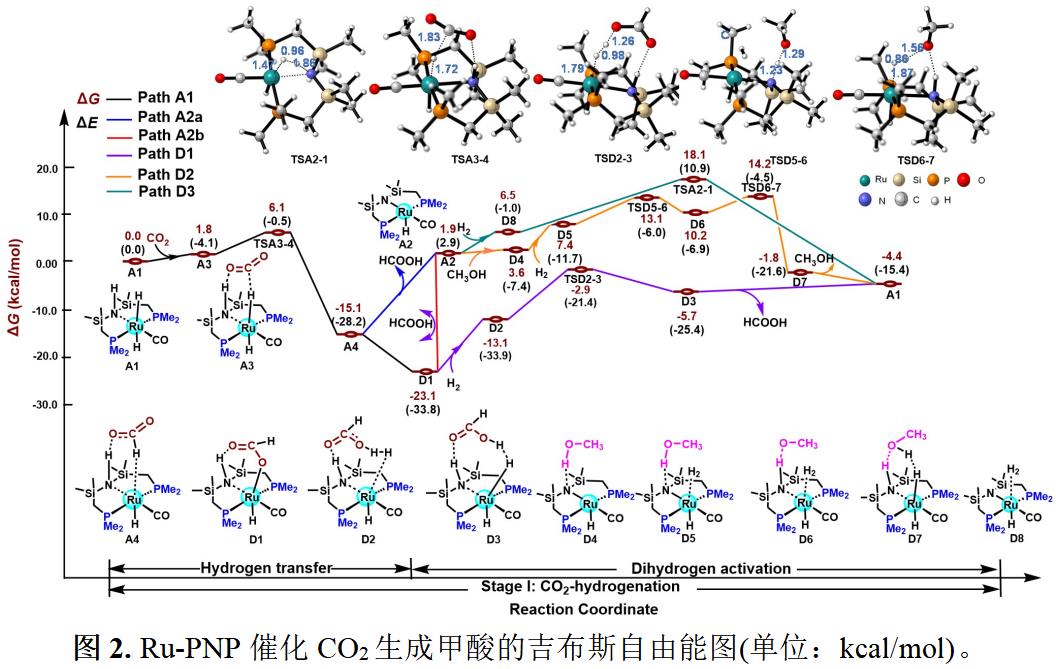
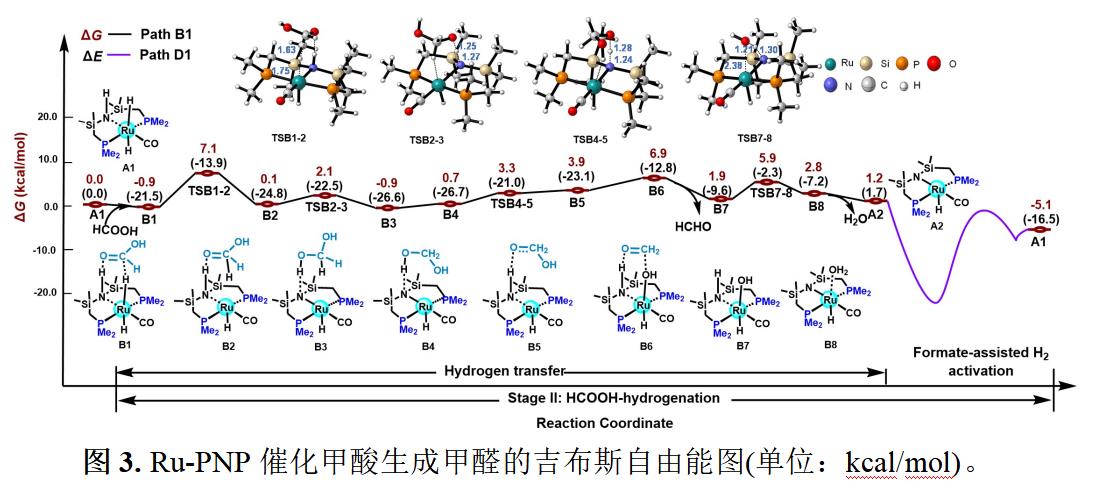
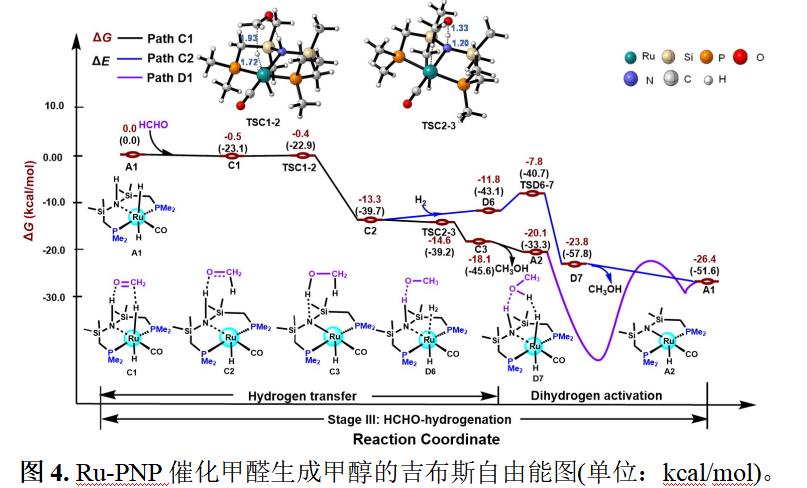
本文分别研究了三个反应阶段(三个反应循环)的反应机理(图2,图3和图4)。计算结果表明,各阶段中,优势路径分别为Path A1, Path B1和Path C1。由于含甲酸分子的配合物D1的稳定性,本文提出甲酸盐辅助氢气活化反应步骤可能是A2再生为A1的主要氢气活化的催化活性组分的再说策略,反应自由能能垒为20.2 kcal/mol,且为各个阶段优势路径中的速控步。
同时,本文也探究Ru-PNP配合物催化酮加氢的可能性,探究了Ru-PNP催化丙酮加氢的反应机理。同时提出,该Ru-PNP具有氢气加氢和转移加氢的催化加氢活性。如果催化活性组分A1的再生可考虑以异丙醇作为氢源,即丙酮加氢的逆反应-异丙醇脱氢过程,此过程的反应自由能能量跨度为16.1 kcal/mol(E3→TSE1-2)。
本研究还研究了溶剂对该反应的影响。计算结果表明,该反应在甲苯中的速度决定步骤仍然是甲酸盐辅助的H2活化步骤,其自由能能垒为22.5 kcal/mol。不同溶剂对反应氢转移模式的影响不同,如甲醇辅助氢气活化过程中,氢负离子转移和质子转移在甲苯溶剂中是同步的,而在甲醇溶剂中是分步的(即质子转移先于氢负离子转移)。
最后,我们还研究了钌螯合物[RuH2(Ph2PCH2SiMe2)2NH(CO)]和[RuH2(Me2PCH2CMe2)2NH(CO)]在三个反应阶段的关键步骤的活化能垒(如表1)。计算得到[[RuH2(Ph2PCH2SiMe2)2NH(CO)]和[RuH2(Me2PCH2CMe2)2NH(CO)]催化甲酸盐辅助H2活化的能垒分别为21.0 kcal/mol和19.1 kcal/mol,都具有较好的催化CO2加氢反应活性。
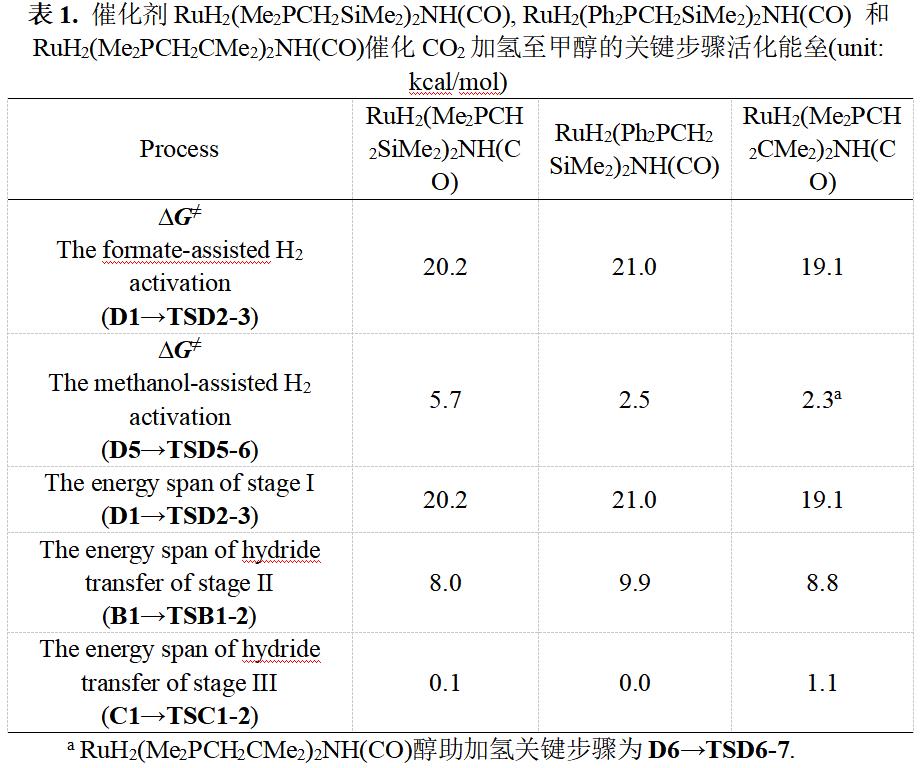
综上所述,该文采用DFT方法对[RuH2(Me2PCH2SiMe2)2NH(CO)] (Ru-PNP)催化CO2加氢制甲醇进行了深入研究。计算结果表明,由于配合物D1的稳定性,甲酸盐辅助H2活化比甲醇辅助H2活化和直接H2活化更有利。甲酸盐辅助H2活化是三个反应阶段的速率决定步骤,能垒为20.2 kcal/mol。同时,钌螯合物既可以H2为氢源驱动二氢加氢,又可以异丙醇等为氢源催化转移加氢。此外,钌螯合物催化剂[RuH2(Ph2PCH2SiMe2)2NH(CO)]和[RuH2(Me2PCH2CMe2)2NH(CO)]在CO2加氢制甲醇方面也具有一定的潜力。该工作为设计用于二氧化碳和C=O转化的过渡金属催化剂提供了理论依据。该文的第一作者为计算化学所2018级本科毕业论文生周颖同学。此工作获得了国家自然科学基金面上基金项目的支持。