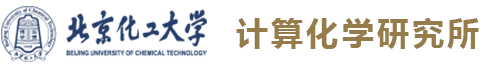氟原子的强电负性、较小半径,使其在药物化学中可以发挥显著的作用。氟原子常用于药物化学中以提高效力、代谢稳定性、降低毒性等。据统计,过去30年开发的药物中有18%含有氟原子。鉴于日益增长的需求,科学家们致力于为含氟分子提供有效的合成方法。羧酸已被广泛用作引导或活化基团以促进键断裂和形成反应。通过利用羧基作为无痕合成工具,可以提供极大的合成灵活性。作者设想利用脱羧反应来立体专一实现烯基氟化物的合成。此外以立体专一的方式合成氟代烯烃且需要避免顺反异构化,表现出该策略的挑战性和重要性。该策略的另一个目标是对氘代氟烯烃的便捷合成。氘同位素标记在广泛的研究领域中发挥着至关重要的作用,特别是对于药物化学家而言:利用更强的碳-氘键替换碳-氢键,通常可以改善化合物的吸收、分布、代谢、排泄和毒性(ADMET)特性。由于在氨基酸的α-位进行氘代标记已被证明具有挑战性,本策略所得到的氘代氟烯烃可作为氘代酰胺生物电子等排体结构研究。
Scheme 1. Bioactive alkenyl fluorides(来源:Journal of Catalysis)
基于此,北京化工大学谭嘉靖课题组与雷鸣课题组合作发展了一种银催化的脱羧质子化/氘代反应,可以从获得的氟代烯基羧酸制备末端单氟烯烃及其氘代类似物。该策略具有操作简单、底物适用广、效率高和立体选择性专一的特点,是对现有方法的有效补充。该研究成果近期发表在Journal of Catalysis上(2022, 413, 1089-1097. DOI: 10.1016/j.jcat.2022.08.008)。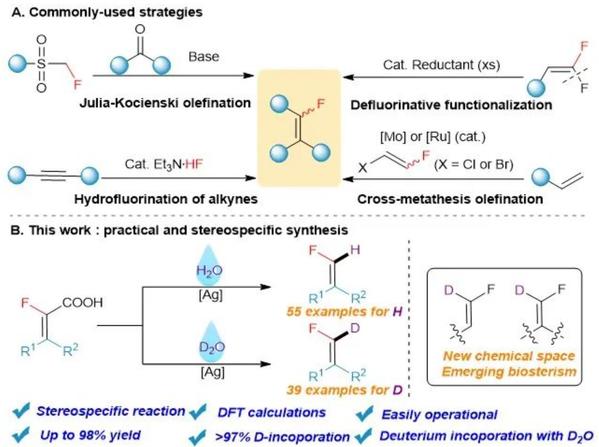
Scheme 2. Working hypothesis(来源:Journal of Catalysis)
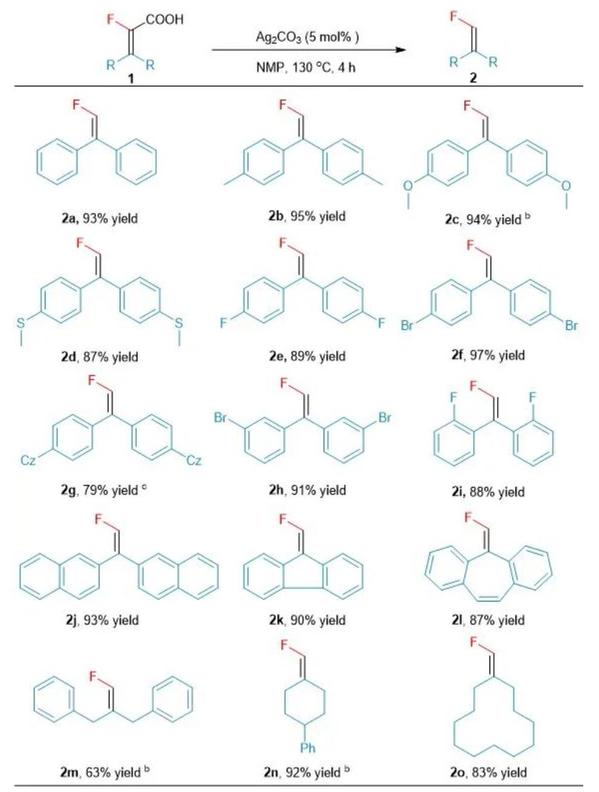
在最优条件的基础上,作者考察了该反应的普适性。在最佳条件下,探究对称酮衍生底物的范围,以良好收率将α-氟丙烯酸转化为三取代的末端烯基氟化物。给电子基团和吸电子基团都具有良好的耐受性,均能以良好的产率得到目标产物。同时,取代基的位置对反应没有较大的影响。进一步研究表明,在以前的报告中具有挑战性的脂肪族底物也可以在10%的催化剂条件下以中等收率(63-92%)得到对应的产物(Scheme 3)。Scheme 3. Substrate scope a. aReaction conditions: Ag2CO3(5 mol%), 1 (0.2 mmol), NMP (1 mL), N2, 130 ℃ oil bath for 4 hours. b10 mmol % Ag2CO3. cCz = Carbazole.(来源:Journal of Catalysis)
紧接着,作者对不对称二芳基醛和酮衍生的氟代丙烯酸范围也进行了拓展。首先,一系列在芳基上具有不同取代基的反式E-氟代烯烃很容易以良好的收率获得(4a-4m-E, 78%-98%),其E/Z比与其反应物基本相同。值得注意的是,具有Z构型的底物由于活性较低,需要在标准条件下适当延长反应时间,最终也立体保持地进行了脱羧(4m-4t-Z, 73%-86%),进一步证明了该策略的合成优点。此外,许多具有其他官能团的分子(包括醚、酰亚胺和烯烃)对该体系也适用,以良好的收率和Z/E比(4aa-4ad-E)提供目标产物。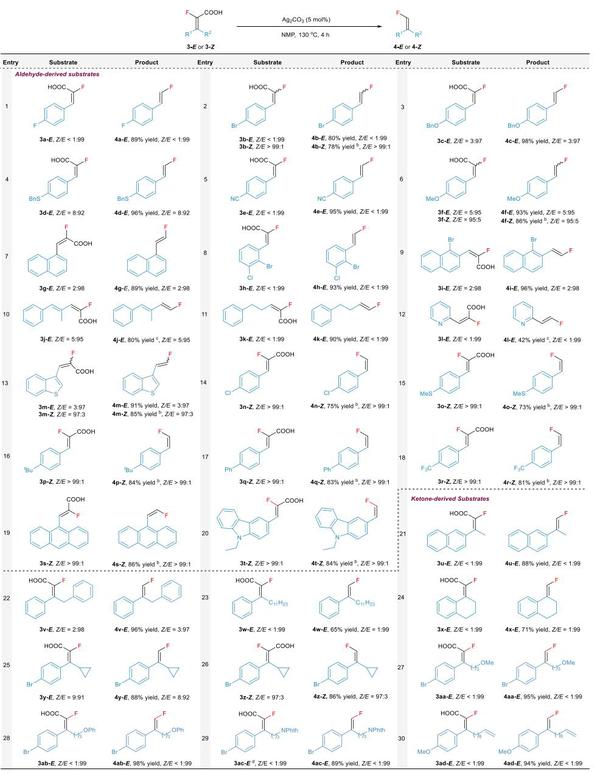
Scheme 4. Substrate scope a. a Reaction conditions: 3 (0.2 mmol), Ag2CO3 (5 mol%) in 1 mL NMP under N2 atmosphere, 130 ℃ oil bath for 4 h. b 12 h. c Using 10 mol% Ag2CO3. d NPhTh = Phthalimide.(来源:Journal of Catalysis)
随后,作者利用该策略对功能分子进行修饰(Scheme 5)。常用除草剂苯草酮成功地以较高产率转化为氟代烯烃6a-Z和6b-E。衍生自药物分子非诺贝特的底物也以良好的收率提供目标产物,并且脱羧反应在烯基位置选择性地进行,而脂肪族羧基官能团保持完整(5d-Z和5f-E)。Scheme 5. Derivatization of functional compounds a. a Reaction conditions: 5 (0.2 mmol), Ag2CO3(5 mol%) in 1 mL NMP under N2 atmosphere, 130 ℃ oil bath for 4 h. b (I) Fluorescence emission of TPE-CHO and 6g; (II) 6g in THF/water mixtures, concentration: 5 μM; excitation wavelength: 330 nm.(来源:Journal of Catalysis)
完成了脱羧质子化的探索,作者进一步进行该策略脱羧氘代的探究。通过简单地添加重水作为添加剂,可以获得与脱羧质子化相近的分离产率和E/Z比的氘代产物及良好的氘代率(Scheme 6)。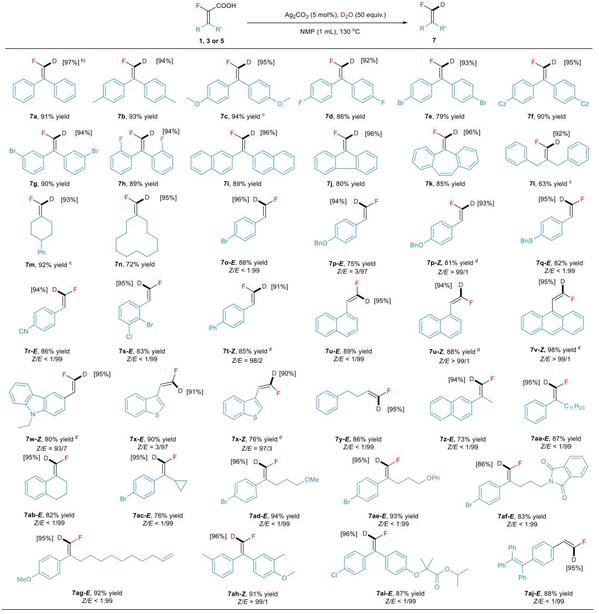
Scheme 6. Deuterated substrate scope a. a Reaction conditions: substrate (0.2 mmol), Ag2CO3(5 mol %), and D2O (50 equiv.) in 1 mL NMP under N2atmosphere, 130 ℃ for 4 h. b D-incorporation ratio determined by 19F NMR. c Using 10 mol % Ag2CO3. d 12 h.(来源:Journal of Catalysis)
雷鸣教授团队采用DFT(密度泛函理论)方法计算了银催化氟代烯烃脱羧反应的机理。计算研究了4种可能的反应机制,包括E构型底物参与的缔合(Path A1)和解离机制(Path B1)、Z构型底物参与的缔合(Path A2)和解离路径(Path B2)。计算结果表明:在所有的反应路径中,脱羧步骤均为反应的决速步骤,E构型底物比Z构型底物更具反应性,且它们都倾向于缔合机制(Path A1和Path A2)而不是解离机制(Path B1和Path B2)。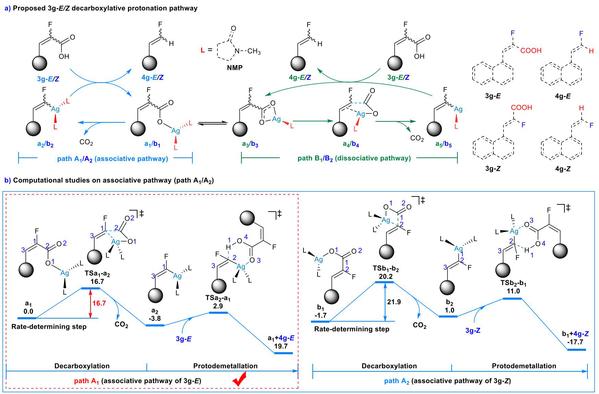
Scheme 7. a Proposed 3g-E/Z decarboxylative protonation mechanism. b Relative Gibbs free energies (in kcal/mol) of 3g-E/Z associative decarboxylative protonation mechanism.(来源:Journal of Catalysis)
DFT同时进行了自然键轨道(NBO)和二阶微扰能量分析以阐明不同底物参与的催化反应活性。对于过渡态TSa1-a2,σ(Ag-C1)→σ*(C2-O1 + C2-O2)重叠有助于Ag-C1和O1-C2-O2供体-受体相互作用,该作用具有44.8 kcal/mol的二阶微扰能(E2)。对于TSb1-b2,σ(Ag-C1)→σ*(C2-O1 + C2-O2)(E2 = 52.6 kcal/mol)提供了比其对应的TSa1-a2更强的轨道相互作用。轨道相互作用的这种差异导致在脱羧步骤中TSa1-a2的C1-C2键断裂比TSb1-b2中的断裂更容易。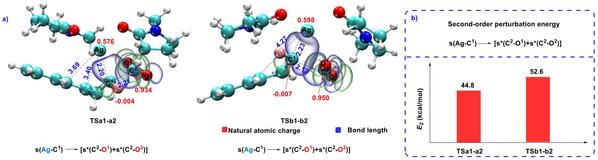
Scheme 8. Natural bond orbital (NBO). a NBOs participating in the C1-Ag and O1-C2-O2 donor-acceptor interactions of TSa1-a2 and TSb1-b2 (unit of bond length: Å). b Second-order perturbation energy of the NBOs.(来源:Journal of Catalysis)
综上所述,作者通过使用银催化的脱羧策略,实现了立体保持的末端单氟烯烃衍生物的合成。此外,通过使用廉价易得的重水作为氘源,实现了氘代类似物的合成。广泛的底物范围、功能分子的多样化和放大的可行性进一步证明了合成价值。计算分析二氧化碳脱除为速率决定步骤,并揭示缔合机制更有利。同时利用自然键轨道(NBO)和二阶微扰能量分析以阐明不同底物参与的催化反应活性。此后,目前正在努力开发其他脱羧官能化反应。该策略将扩大合成产品范围,并促使新的生物等排体研究作为基础。上述研究工作得到了国家自然科学基金、中央高校基本科研业务费等项目的资助。